ここから本文です。
![]() 2019年04月16日
福祉保健局
2019年04月16日
福祉保健局
医薬品成分を含有する製品の発見について
都では、いわゆる健康食品による健康被害発生の未然防止のため、都内で販売等される製品の調査及び成分検査を行っています。
平成31年3月26日に「医薬品、医療機器等の品質、有効性及び安全性の確保等に関する法律」(以下、「医薬品医療機器等法」という。)違反で都内事業者に対して措置を行いました(平成31年3月27日付報道発表)。その際、違反品と類似の下記1製品を発見したため任意提出を受け成分検査を行ったところ、医薬品成分である「ノルカルボデナフィル」が検出されました。
当該成分を含む下記製品は医薬品に該当し、厚生労働大臣の承認を受けずに製造販売することは、「医薬品医療機器等法」で禁止されています。
なお、これまでに当該製品による健康被害発生の報告は受けていません。
製品概要
| 表示内容 | 品名 | BARIKATA |
|---|---|---|
| 名称 | 植物混合末加工食品 | |
| 販売者 | 株式会社●● | |
| 東京都●●区 | ||
| 製造者 | 株式会社●● | |
| 東京都●● | ||
| 原材料名 | 植物混合末(トンカットアリ粉末、マカ粉末、ガラナ粉末、コーヒー豆末)、結晶セルロース、ステアリン酸カルシウム | |
| 内容量 | 0.75グラム(375ミリグラム×2粒) | |
| 消費期限 | 2021年3月3日 | |
| 形状 | カプセル | |
| 検出成分 | 1カプセル中「ノルカルボデナフィル」を6.9ミリグラム検出 | |
試験実施機関
東京都健康安全研究センター
根拠条文
医薬品医療機器等法第55条第2項(無承認医薬品の販売・授与等の禁止)
都民の皆様へ
当該品の摂取により健康被害を受ける可能性が否定できませんので、当該製品をお持ちの方は、直ちに使用を中止してください。また、健康被害が疑われる場合には、速やかに医療機関を受診してください。
なお、ノルカルボデナフィルは、ED治療薬として承認されているシルデナフィルの類似化合物です。国内では、ノルカルボデナフィルを配合した医薬品は承認されていません。
都の対応
- 製品を販売した都内店舗(●●区)に対し、販売中止及び自主回収を指示しました。
- 製品に表示された製造業者(●●)に対し、製造中止、出荷中止及び廃棄処分を指示しました。
- 関係団体へ注意喚起のため情報提供しました。
現品写真(現品は薬務課で保管しています。)



参考
ノルカルボデナフィルは、シルデナフィルと類似の化学構造であり、類似の作用を有することが考えられるため、健康被害が発生するおそれが否定できません。国内ではシルデナフィルのクエン酸塩が医薬品(販売名:バイアグラ錠等)として承認されています。なお、承認されているシルデナフィルクエン酸塩の主な適応と主な副作用は、次のとおりです。
- 適応
勃起不全(満足な性行為を行うに十分な勃起とその維持が出来ない患者) - 副作用
血管拡張、頭痛、動悸等 - 添付文書上の警告(概要)
高血圧及び狭心症の薬である硝酸剤あるいは一酸化窒素(NO)供与剤(ニトログリセリン、亜硝酸アミル、硝酸イソソルビド等)との併用により降圧作用が増強し、過度に血圧を下降させることがあるので御注意ください。
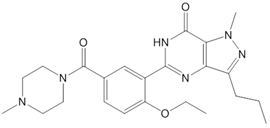
ノルカルボデナフィル
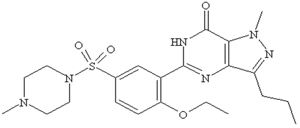
シルデナフィル
| 問い合わせ先 福祉保健局健康安全部薬務課 電話 03-5320-4512 |
Copyright (C) 2000~ Tokyo Metropolitan Government. All Rights Reserved.